多肽Tβ4还能为医药市场带来多少想象空间?

图片来源:Unsplash-Christina Victoria Craft
文|动脉新医药
RegeneRx Biopharmaceuticals Inc.(以下简称:RegeneRx)于1982年成立于美国马里兰州,是一家公开上市的、处于临床阶段的生物制药公司。
该公司擅长于生物组织的保护、修复和再生,专注研究和开发新型多肽药物,以保护和修复由疾病、创伤或其他病理因素造成的组织和器官损伤。
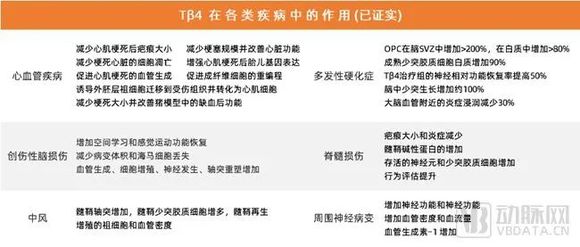
RegeneRx董事会主席兼前席科学顾问Allan Goldstein博士开发出的一种新型治疗肽胸腺肽β4(Tβ4)为该公司核心技术。围绕组织和器官的保护、修复和再生,现已将Tβ4衍生出三条主管线。
1982年,J. J. Finlelstein创立RegeneRx,并担任总裁兼首席执行官。Finlelstein先生拥有德克萨斯大学金融学商业学位,一直负责美国和其他国家多种医疗器械的监管审批和营销,也在担任生命科学行业执行官与顾问方面拥有几十年的经验。
而Goldstein博士自1982年公司创立以来一直担任董事会主席兼首席科学顾问。同时他还是一名生物化学教授,1978年往后的31年时间里,担任乔治华盛顿大学医学与健康科学学院生物化学和分子生物学系主任。
Goldstein博士在生物化学,免疫学,心脏病学,癌症和伤口愈合方面拥有超过25项已颁发和/或正在申请的专利,累计发布期刊类文章430余篇。博士是几种重要化合物的发明人,包括在全球范围内销售的T a1和作为RegeneRx临床项目基础的T 4。
1990年代,Finlelstein先生曾短暂离开该公司并领导另一家生物医药公司,Goldstein博士暂时接管其职务。2002年,Finlelstein先生带着这10年的宝贵经验,再次回到RegeneRx,恢复原有职位。
Finlelstein先生回归后的次年10月,RegeneRx宣布在OTCQB上市(otcqb:RGRX),后续共开展8次融资,累计收获1175万美元。
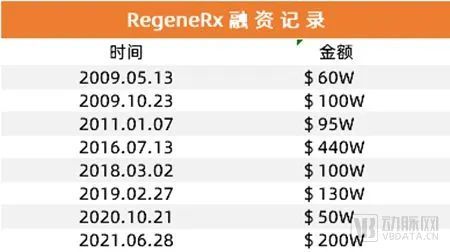
RegeneRx融资记录(数据来源:Crunchbase)
RegeneRx目前专注于将三种基于Tβ4的独特候选药物推向临床:RGN-137、RGN-259和RGN-352。
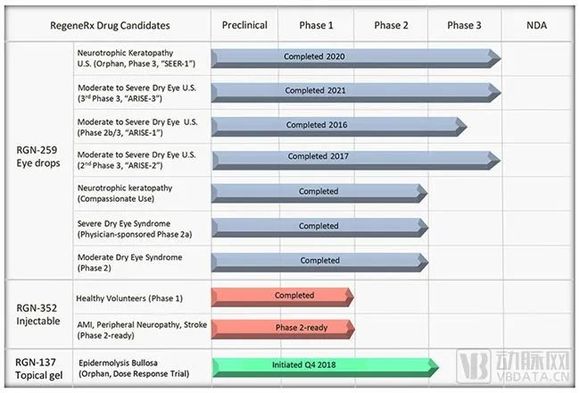
RegeneRx三大主要管线进度表
1、RGN-259
RGN-259为公司的首要开发项目,是一种基于Tβ4的无菌且无防腐剂滴眼液,可治疗干眼病(DED)和神经营养性角膜炎(NK)。
Tβ4能够促进细胞迁移,通过增加层粘连蛋白-5的产生增加细胞-细胞和细胞-基质的接触,并减少角膜中的细胞凋亡和炎症。目前市面上还没有显示出角膜修复和抗炎特性的药物,RGN-259为角膜愈合提供了新思路。
干眼症治疗的相关临床试验表明,与安慰剂相比,0.1%RGN-259的DED体征和症状都有许多统计学上的显着改善,同时显示出出色的安全性,舒适性和耐受性。对于体征,RGN-259还改善了干眼症患者在角膜荧光素染色受损和阻止病情恶化的能力。
RGN-259也被用于治疗溃疡型神经营养性角膜炎(NK),这是一种由糖尿病和带状疱疹病毒引起的持续性角膜缺陷。2013年12月,RegeneRx从美国FDA获得了用于治疗NK的RGN-259的孤儿药批准。在临床试验中,使用RGN-259的NK患者能够在约四周时间得到痊愈。
2、RGN-352
RegeneRx正在开发RGN-352,这是一种可注射的Tβ4制剂,用于治疗全身组织和器官损伤,包括心脏,神经系统,肺部和肾脏病变。许多心脏损伤动物模型已经表明RGN-352在减少疤痕量、增加心脏功能和生存方面的有效性。
现有临床前研究已经表明,Tβ4具备刺激干细胞分化,减少细胞凋亡和炎症,保护细胞免受细胞毒性,增加血管生成和减少动物模型中疤痕形成的能力。基于动物模型方面的工作,最近发表的科学论文表明,Tβ4可以预防或减少对肺部和肾脏的损害,是全身炎症反应综合征(SIRS)和败血症的患者,以及COVID患者。
RGN-352在4个剂量水平下均被证明是安全的和耐受性的。RegeneRx将来自NIH国家心脏、肺和血液研究所的300万美元赠款用于进行许多其他动物毒理学和药代动力学研究,以支持人体临床试验。RGN-352现已经准备在进行2期临床试验。
3、RGN-137
RegeneRx一直在开发RGN-137,一种肽Tβ4的局部凝胶制剂,作为加速真皮伤口愈合的新型治疗方法。据美国国立卫生研究院调研,RGN-137是第一个用于人体临床试验的Tβ4的制剂。
与生长因子不同,RGN-137在临床前研究中已被证明可以减弱多种愈合途径,例如细胞凋亡,血管生成,胶原蛋白沉积和组织炎症。在临床前研究中显示,当损伤发生时,Tβ4的基因是最早上调的基因之一,这表明Tβ4肽有助于愈合过程。
2009年完成了两项2期盲法、安慰剂对照、剂量反应的临床试验,用于治疗晚期压疮和静脉淤滞性溃疡。一项关于治疗大疱性表皮松解症(EB)的2期盲法安慰剂对照试验于2011年年中完成。在所有三项试验中,中剂量组在加速愈合方面表现出最大的活性;在任何剂量或任何患者群体中均未发现严重不良事件。
3期临床试验已于2018年获得FDA批准在EB患者中展开,EB是一种导致皮肤和内脏严重起泡的遗传性疾病。
迄今为止,已有超过1700名患者接受了RegeneRx基于Tβ4的产品配方的测试,这些配方局部施用于皮肤,眼睛,并注射到血液中。这些制剂没有产生严重的不良事件,并且在迄今为止的每项临床研究中都被认为是安全和耐受性的。
RegeneRx成立至今已有40年,目前在全球四个主要地区拥有积极的合作伙伴关系:美国和加拿大,中国(泛亚洲)和欧盟。其中,该公司的中国合作伙伴目前正准备在中国发起一项用于治疗干眼症RGN-259管线的2/3期临床试验。
2012年,RegeneRx与李氏制药公司(Lee's Pharm)签订了许可协议,在中国开发和销售Tβ4相关产品。Lee's将负责许可区域的产品开发,各方将共享与这些产品候选产品相关的临床和其他数据。近期,Lee's在中国建立了新的眼科制造工厂,加速了RGN-259的开发。
2014年,RegeneRx与韩国生物技术公司HLBT(前身为 GtreeBNT)签订了战略合作协议,在韩国,日本和澳大利亚等28个亚洲国家开发和营销RGN-259。HLBT还将在美国开发RGN-137用于真皮伤口愈合。2017 年 8 月,RegeneRx又与 HLBT修订了 RGN-137 许可协议,将区域扩展到包括欧洲、加拿大、韩国、澳大利亚和日本。
以往几十年的基础科学研究已经开发出Tβ4在众多适应症中的开发潜力。接下来RegeneRx将着重推进其现有管线的晚期临床试验和产品商业化,同时也将着手开发新适应症的临床管线。
RegeneRx始终保持寻找在所需药物治疗领域具有临床开发和商业化兴趣的公司进行战略合作,同时也在其重点疾病领域积极寻求基础设施、专业知识方面的长期合作伙伴。RegeneRx将继续保持其发展战略,将部分候选产品的开发和商业化权利授予拥有开发其候选药物的专业知识和资金的合作伙伴。