未来,P53究竟会成为下一个广谱抗癌药,还是继续吞噬药企的研发黑洞?

文|氨基财经 方涛之
在人类2-3万个基因组中,TP53基因绝对是一个令医学界又爱又恨的存在。
令人爱的是,TP53所编码的P53蛋白,会在人体内兢兢业业,寻找并修复那些被损伤的DNA,避免其带领细胞走向歧途成为癌细胞。
令人恨的是,这些本该守护人体基因的P53蛋白又时常掉链子,出现一些没有活性甚至帮助癌细胞的突变型。并且,P53突变广泛存在,在超过50%的癌细胞中,都发现了突变的P53蛋白。这也让P53看上去是一个极具潜力的广谱抗癌靶点。
但历经40年,人类对这些突变的P53蛋白还束手无措,至今仍未有P53药物获批上市,罗氏、强生、诺华等大药企纷纷折戟于此,强生、默沙东也先后宣布暂停相关的研究项目。
P53早已被行业定义为极难攻克的靶点之一。然而,面对不可成药的P53及其潜在广谱特性,仍有不少海内外药企继续挑战。PMV公司以及亚盛医药,均在ASCO年会上披露了最新临床数据,且初步表现出不错的潜力。
未来,P53究竟会成为下一个广谱抗癌药,还是继续吞噬药企的研发黑洞?
我们都知道,癌症其实是人类体内基因突变产生的恶果。
不过,面对可能潜在的基因突变风险,人体也并未坐以待毙。在人体内有不少抑癌基因,一直在与可能发生的基因突变作斗争。
具体来说,在癌症的发生和发展过程中离不开两种类型的基因,一种是致癌基因,另一种是抑癌基因。
其中,抑癌基因是人体的健康卫士,一直在为保卫我们的健康不断奋斗。在众多的抑癌基因中,TP53是最为人所熟悉的健康卫士之一。
早在1979年,科学家便鉴定出TP53基因所编码的P53蛋白。更准确地说,鉴定出的是具有致癌作用的P53突变蛋白株。
这也使得原本具有抑癌作用的P53蛋白被误解了近十年。直到1989年,科学家终于为野生型P53正名。
科学家发现,野生型P53不但不会致癌,反而是人类对抗癌症的好帮手。它能够调控细胞周期,帮助修复损伤的细胞DNA,还能够使得受损细胞凋亡。
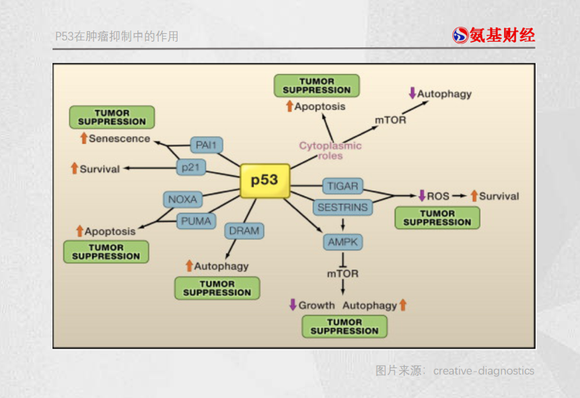
也正因此,P53也被形象地称为“分子警察”。
作为“分子警察”的P53蛋白每天都在勤劳巡逻,检测人体中是否有因为辐射、氧化、致癌等因素损伤的DNA。一旦发现,P53就会在它们细胞分裂前进行修复,以免损伤的DNA导致细胞出现癌变的风险。
如果P53发现有一些冥顽不灵的DNA,在修复后仍会引发细胞癌变,或者根本无法修复,P53就会诱导这些损伤的细胞凋亡。
那么,既然有P53这个“分子警察”在,为什么人体的细胞还是会出现癌变呢?原因之一在于,P53的队伍中也会出现“叛徒”。
有的P53蛋白会出现突变,突变后其空间构象发生了改变,也就失去了活性。此时的P53非但不能抑制癌细胞的生长,反而会助纣为虐,成为致癌的推手。比如,诱导对癌症药物的耐药性、促进肿瘤扩散、生长,抑制癌细胞凋亡、促进癌细胞内血管生成等。
研究发现,在大约50%的癌细胞中都发现突变P53的存在。因此,如何拯救“堕落”的分子警察,使得P53恢复其原本功能,成了癌症药物研发的重要课题。
遗憾的是,P53虽已被发现40余年,但目前为止围绕P53研发的药物都以失败告终。
因为,要想恢复P53药物的活性困难重重。
首先,开发靶向P53的药物需要激活蛋白的活性。然而,激活蛋白的活性要比抑制蛋白活性难得多。毕竟让坏人学好,可比让好人学坏要难得多。
而且,在激活蛋白活性这方面,也没有什么成功的例子可以借鉴。目前为止,靶向抑癌蛋白的药物研发几乎没有什么成功的案例。
根据《自然》杂志的一项研究,临床上100多个靶向药物几乎都是靶向致癌蛋白的,并没有一种是靶向抑癌蛋白的。
说白了,“复活”P53这条路到底能不能走得通,还是个未知数。
已经有不少药物,在恢复P53活性的路上栽了跟头。比如,曾经备受期待的Eprenetapopt就是一个典型案例。
从机制上来说,Eprenetapopt能够重塑突变折叠错误的P53蛋白,将其重新激活为野生型结构,从而发挥其抑癌作用。
这个机制不仅听上去神奇,在治疗TP53突变的骨髓增生异常综合征或急性髓细胞白血病的临床1b/2期研究中,也确实展现出了一定的效果。
但在2020年12月28日,Aprea Therapeutics公布,Eprenetapopt临床Ⅲ期研究并没有达到临床终点。这也使得Aprea Therapeutics的股价暴跌78.08%,由前一日的25.09美元/股跌至5.5美元/股,目前其最新股价不足1美元。这便是新药研发的“残酷”之处。
其次,更艰难的是,P53是与RAS、MYC齐名的三大不可成药靶点之一。P53蛋白的表面光滑,没有合适的口袋能够与化合物结合,这也使得P53很难成药。
不过,只要思想不滑坡,办法总比困难多。
对于这些难题,不少药企选择“曲线救国”,通过抑制P53与其他蛋白的结合来恢复P53的功能。
其中,MDM2成为了不少药企的选择。MDM2是P53的关键负调节因子,在正常细胞中MDM2会介导P53的降解,使得P53蛋白维持在低水平。
罗氏的RG7112就是一款MDM2抑制药物,其通过抑制MDM2,来抑制MDM2降解P53。不过,在临床试验中,患者需要服用高剂量的RG7112才能起效。而高剂量的药物带来了胃肠道毒性、中性粒细胞和血小板减少等多种毒性。因而,需要更为有效的MDM2抑制剂,才能减少药物毒性。
为此,罗氏又开发了强效MDM2抑制剂Idasanutlin。
Idasanutlin通过选择性结合MDM2表面的P53位点,使得MDM2无法与P53结合,P53也就无法被降解。留下来的P53便可以继续行使监督功能,杀死那些具有癌变倾向的细胞。
彼时,人们对这一药物寄予厚望。在媒体评选的2019年最具潜力的创新药中,Idasanutlin赫然在列。
但就在2020年,罗氏的强效口服MDM2蛋白抑制剂又一次失败了。
罗氏也并非大药企中唯一在P53蛋白上折戟的。
过去的十几年里,如强生、赛诺菲、默沙东都曾在这个靶点的研究上铩羽而归。基于此,P53一度被认为可能是一条“死胡同”。
好在,仍然有一些人在坚持破解这个不可成药靶点。
近期,一些药企的研发又为P53近四十年的研发之路,带来了一丝曙光。
比如,PMV公司的PC14586就是一款初具潜力的P53激活剂。在今年ASCO年会议论文摘要中,PC14586交出了一份看起来很不错的答卷。
PC14586是一款P53突变Y220C激动剂。P53突变体种类繁多,迄今为止已发现超过 25000个独特的P53突变,若是想要一刀切来解决所有的突变体,可能性并不大。
所以,PC14586选择以P53众多热点突变中的Y220C突变来下手。PC14586通过选择性地纠正由特定P53突变Y220C引起的P53错误折叠,同时保留野生型P53,以达到恢复P53活性、抗肿瘤的作用。
简单来说,就是将坏掉的P53结构恢复。
根据PMV公司披露的临床数据,截至2月8日,在29例既往接受过3线以上治疗的患者中,21例可评估效果的患者中有5例,也就是23%的患者达到了部分缓解。
这5例患者中,包括小细胞肺癌、乳腺癌、结直肠癌、前列腺患者。这也说明,未来P53激动剂很有可能成为一个广谱抗癌药。而这也正是吸引众多药企前赴后继开发P53的重要原因。
在安全性方面,PC14586初步表现良好,79%的患者中观察到治疗相关不良反应。其中两位患者是3级不良反应,其余均为以、1/2级不良反应。
无论是广谱性还是安全性,PC14586均初步展现出效果。
在国内,也有一些玩家致力于P53靶点研发,比如德琪医药、亚盛医药、赛百诺等等。其中,亚盛医药研发的MDM2抑制剂APG-115,在ASCO年会官网上公布了最新的临床研究摘要。
摘要显示,在APG-115联合K药治疗成人及儿童实体瘤患者的II期临床中,对PD-1/PD-L1抑制剂耐药的黑色素瘤队列中38个病人疗效可评估,客观缓解率为为13%。其中,有2例患者完全缓解,皮肤黑色素瘤和葡萄膜(眼)黑色素瘤亚组的客观缓解率分别为24%和9%。
在PD-1 / PD-L1抑制剂耐药的NSCLC、尿路上皮癌和脂肪肉瘤队列中,分别有1例确认PR(部分缓解)。这也初步说明,APG-115对于多个癌种都有抗肿瘤活性。
未来,这些后来者能否改变P53不可成药的命运还未可知。但可以确定的是,一旦成药,将意味着一款新的重磅靶向药物为癌症患者带来希望,同时也将为药企带来可观的回报;反之,等待药企的可能是研发费用付诸东流,甚至如Aprea Therapeutics般的暴跌。
但在一款潜在“不限瘤种”的广谱抗癌药面前,这些风险总是值得的。