细胞培养肉是怎么一回事,既然有了植物肉和发酵蛋白肉,为什么还需要细胞培养肉?

文|FoodPlusHub Turo
“我们不应为了吃鸡胸肉或鸡翅而养一整只鸡,应该在合适的培养基中分别培养这些组织”,出于动物福利和生产效率方面的考量,英国前首相丘吉尔在1931年曾这么畅想过。
在近一个世纪后,丘吉尔当初这个“狂野”的畅想已经成为了现实,而这个现实背后是正在发生的全球蛋白质的供应系统的革命。
风险资本的热情往往可以充当着一个早期行业的风向标,我们可以通过资本的动态见微知著来感受一个早期行业的脉搏与能量。
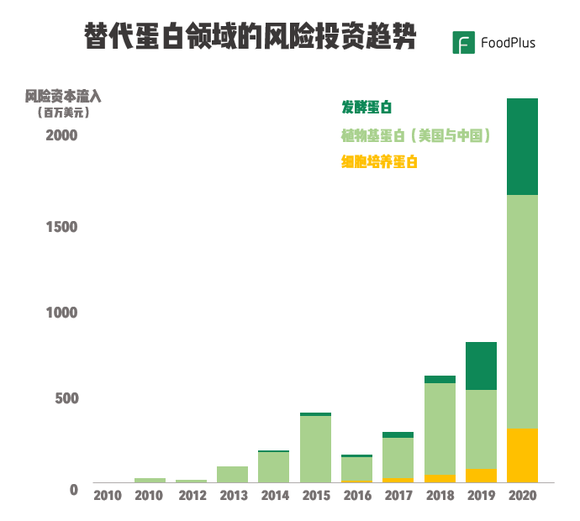
替代蛋白领域的风险投资趋势,来源:Crunchbase, GFI, FoodPlus
2020年,细胞培养蛋白领域的投融资金额实现了近400%的增长,总金额超过了4亿美元,这个增速远超植物基蛋白和发酵蛋白领域。
尽管已经增速惊人,但我们可以负责任地说:2020年只是一个开始。我们在《是时候聊聊我们对发酵替代蛋白万亿市场背后机会的观察了》中曾做出过一个判断:
替代蛋白与新能源市场相比,整体潜在市场规模相差不大,但资本投入却相差了好几个数量级。从这个角度看,替代蛋白领域的资本投入存在着结构性的缺失,未来将呈现指数级别的增长。
这个判断在今年年初很快就得到了初步验证。单看细胞培养肉,2020年12月新加坡通过全球首个细胞培养肉产品的食品安全监管审核宛如一声声势滔天的冲锋号,点燃了创业公司和资本端的极大热忱。在那之后,尽管遇上了西方人的“圣诞-新年假日季”,短短不到3个月里发生了数起大大小小的投融资事件:
2020年12月7日,荷兰细胞培养肉公司Mosa Meat宣布完成了B-2轮融资,筹集了2000万美元,其B轮融资额累计达到7500万美元;
2021年1月13日,澳大利亚细胞培养肉公司Vow Food近日完成了600万美元的种子轮融资(Vow Food的特别之处在于他们重点关注的是非驯服动物,如袋鼠肉、羊驼、水牛,甚至是已经灭绝的动物);
2021年1月19日,美国的细胞培养海鲜公司BlueNalu获得了6000万美元的债务融资;
2021年1月21日,西班牙的细胞培养肉公司BioTech Foods表示他们正在领导一个520万欧元的细胞培养肉项目,这个的启动资金中有370万欧元是西班牙政府出资;
2021年1月26日,瑞士的细胞培养肉创业公司Mirai Foods完成了240万美元的种子轮融资。Mirai Foods成立于2019年,目前主攻细胞培养牛肉,开发出原型产品只用了6个月,这个时间比先行者们缩短了很多;
2021年2月2日,以色列细胞培养肉企业Future Meat Technologies宣布获得了新一轮近2700万美元的战略融资,投资方包括泰森食品(全球最大的肉类生产商及供应商之一),ADM(全球四大粮商之一),穆勒集团Müller Group以及众多知名食品农业科技风投基金,其中还包括了中国首支专注食品农业科技早期项目投资的VC食芯资本Bits x Bites;
2021年2月11日,加州的细胞培养-植物基混合人造肉创业公司New Age Meats完成了200万美元的补充融资。
2021年2月23日,Mosa Meat完成了1000万美元的B轮补充融资,B轮融资累计达到8500万美元。
这股巨大的能量也传到了中国:
2020年12月21日,南京的细胞培养肉科技公司周子未来宣布获得2000万元天使轮融资,由经纬中国独家投资,这是截至目前中国细胞培养肉领域最大的一笔投资;
2020年12月22日,细胞培养肉品牌CellX宣布完成了数百万元种子轮融资。本轮融资由替代蛋白主题基金力矩中国(Lever VC)领投,英国Agronomics,德国Purple Orange Ventures以及智利Humboldt Fund等跟投;
2020年1月26日,越南越南最大的水产品加工商Vinh Hoan Corporation (VHC) 近日宣布通过收购Avant Meats的股东之一Vinh Technology的方式,获得了Avant Meats的小部分股权。Avant Meats是位于香港的细胞培养海鲜肉创业公司。VHC表示会利用自己的全球销售网络和生产基础设施建设帮助Avant Meats的发展。
希望我们在《是时候聊聊我们对发酵替代蛋白万亿市场背后机会的观察了》中已经达成了一个共识——出于人口增长、气候、土地等要素的限制,传统蛋白质供给系统已经无法满足人类未来的需求,因此一个更环保的、更具生产效率的创新蛋白质供给系统的诞生具有必然性。
2020年替代蛋白产业在全方位都做出了突破,我们能清晰的感受到这种必然性正在不可逆地成为现实。
在三种主流替代蛋白人造肉(植物肉、微生物发酵肉、细胞培养肉)技术中,细胞培养肉是最被寄予希冀的一种,如知名咨询公司科尔尼预测2040年细胞培养肉将达到肉类市场35%的市场份额。在这个细胞培养肉将要迎来小规模爆发的前夕,我们想要先探讨一下细胞培养肉技术的必要性,再从技术、产业链、资本、投资机会、消费者与政策这几个方面简单勾勒出细胞培养肉行业的大致轮廓,让想要进入这个领域创业、从业或者投资的朋友可以快速获得一些认知。
简单来看,细胞培养肉的工业化生产流程为:从动物身上提取活体组织——分离出目标细胞——初步培育目标细胞——将细胞群置入带有培养液的大型培养容器培养——经过10-12天的培养——分离提纯得到细胞培养肉——最终烹饪加工形成终端产品。
上述流程我们会在后面的部分再具体展开介绍,包括目前的核心技术流派、瓶颈以及产业链中蕴含的机会。
细胞培养肉技术实际上并不是什么近年来才出现的新鲜事,这种技术已经存在了100多年,上个世纪也曾有学者在实验室中培养出过“试管肉”(in-vitro meat)。但在当时,并没有需要创造出一种替代肉类的迫切性,很多支撑的理论和技术也没到位,因此这项技术没有得到充分的重视。
如今,寻找到一种替代蛋白已经成为人类必须需要在21世纪解决的一个难题,同时随着各方面的支撑理论和技术的逐渐成熟,通过细胞培养的方式来生产最接近传统肉类的“人造肉”的技术开始得到各界广泛的关注。在2000年前后,学者们阐明了肌肉形成的机理、肌肉干细胞保留了增殖和分化的能力,而组织工程的发展也为培养肉的实现奠定了技术基础。2012年,英国的约翰戈登(John Gurdon)和日本的山中伸弥(Shinya Yamanaka)因发现成熟的成体细胞可转变为多能状态干细胞而获得诺贝尔生理学或医学奖,这一发现有力促进了干细胞学科的发展。
2013年,细胞培养肉领域迎来了一个里程碑事件。荷兰马斯特里赫特大学的Mark Post教授(Mosa Meat的联合创始人与首席科学家)突破了细胞培养肉研发技术路线,分离肌肉和脂肪前体细胞、刺激细胞大量生长,在体外生产三千多条肌纤维,在2013年8月时成功合成了第一块可食用的细胞培养肉,当时他们还为这块来自不易的细胞培养肉举办了电视直播的试吃会。
值得注意的是,这块世界上第一块细胞培养肉饼当时造价32.5万美元。在那之后,各个创业公司苦心研发,试图把成本降下来,但目前纯粹的细胞培养肉产品依旧价格不便宜,2020年年中时Mosa Meat方面表示他们的牛肉产品的成本为每公斤180美元。作为对比,传统畜牧业获得1公斤牛肉需要支出的饲料费用平均是2美元。
可以看出,细胞培养肉是技术研发难度最高的一种人造肉技术,目前也依旧成本高昂。那么,在目前的人造肉技术中,有具有成本与监管审核优势的植物肉,也有具有生产效率与高生物价效(可以理解为吸收率高)的发酵蛋白肉,这种情况下为什么还要砸钱砸时间去研发技术门槛难度最高的细胞培养肉?
主要原因有三个:1.人类写在DNA里的对真实肉类的向往;2.肉中有许多未被发现的营养元素,在体内的代谢流程也没被完全揭示,长期缺乏可能造成身体的某种系统性障碍;3.口味、习惯、心理。
早期人类从大约260万年前就开始把肉类作为常规食物,在这几百万年的漫长进化过程里,对肉的渴望和需求早已被深深写在绝大部分人的DNA里。举个例子,尽管在进化过程中人类的嗅觉退化严重,但现代人类却依旧可以在数公里外闻到烤肉的味道。
上述这种对真实肉类的渴望,很有可能无法被一些替代肉产品完全满足。这一点可以通过代糖来类比。在代糖风靡了一段时间后,如今学术界关于代糖的质疑声越来越大,相关的文献研究的观点主要可分为这三类:
1、代糖通过味觉欺骗人体分泌胰岛素,但这时血糖并没有升高,胰岛素分泌将是并没有升高的血糖水平降低。长时间服用代糖,胰腺将出现适应性现象,出现胰岛素抵抗也就是血糖升高时也不分泌胰岛素,久而久之将导致糖尿病;
2、代糖影响肠道菌群,从而引起血糖耐受量降低,更提出会影响菌群影响的一切功能;
3、代糖不仅不能戒断糖瘾,还会进一步诱发,导致过量食用真糖的倾向。
与糖类似,肉类在人体内的代谢过程远未被完整揭示,此外肉中还有许多未被发现的营养元素,长期进食缺乏某些未知元素的替代肉有造成人体系统性障碍的潜在风险。就算今后植物肉和发酵蛋白肉在口味上可以做到与真肉十分接近,长期食用这些产品还是要面对这种潜在的健康风险,而成分与真肉十分接近的细胞培养肉则可以在一定程度上规避这种风险。目前在一些调研和测评中我们也有听到一种声音:进食植物肉让测评者更加想要吃真肉。

在“为什么你不吃植物肉”的前4个原因中有“不好吃”和“吃不饱”,图片来源:Quartz
此外,心理层面的因素也会造成人体对一些替代肉的排斥。针对这种现象比较有名的一种阐释是“恐怖谷效应(uncanny valley effect)”:
恐怖谷理论是一个关于人类对机器人和非人类物体的感觉的假设,在1970年被日本机器人专家森昌弘提出。其中,“恐怖谷”一词由Ernst Jentsch于1906年的论文《恐怖谷心理学》中提出,而他的观点被弗洛伊德在1919年的论文《恐怖谷》中阐述,因而成为著名理论。
在这种理论里,人会对仿真性高到一定程度但是又不够高的物体产生天然的排斥反应。这种心理现象很早就引起了替代蛋白/人造肉领域的学者和从业人员的注意,而与真肉成分最相近的细胞培养肉被认为是最有可能越过这个“谷”的人造肉技术。
前面我们介绍了细胞培养肉技术的规模化生产流程:从动物身上提取活体组织——分离出目标细胞——初步培育目标细胞系——将细胞群置入带有培养液与“支架”的大型培养容器培养——经过10-12天的培养——分离提纯得到细胞培养肉——最终烹饪加工形成终端产品。
在这个流程中有5个核心要素:种子细胞系、培养液、培养容器、支架、终端产品,在这个部分中我们会具体展开介绍这些要素,包括目前的核心技术流派、瓶颈以及产业链中蕴含的机会。
1、种子细胞系
种子细胞系(cell lines)是细胞培养肉生产流程的基础,许多种类的细胞都可以作为种子细胞系,目前主流采用的细胞种类有肌卫星细胞(Myosatellite cell)、多功能干细胞(Pluripotent stem cells,存在于骨骼肌中)、成纤维细胞(fibroblast,存在于结缔组织中)等。
种子细胞种类的选取基于分化能力与容易程度、增殖速率、基因稳定性等属性,上述这些细胞种类在这些属性中各有优劣。
肌卫星细胞不像干细胞和成纤维细胞一样需要在培养液中加入许多物质来引导分化为肌肉细胞,还有个实践优势是提取与培育相对比较方便。肌卫星细胞的缺点在于增殖速度较慢,并且衰老得比较快。“元老型”细胞培养肉公司Mosa Meat使用的是肌卫星细胞。
多功能干细胞也被一些公司采用作为种子细胞系。多功能干细胞也可以较为容易的分化成肌肉细胞,但是衰老得比较快,并且在实验室里存活困难。
肌卫星细胞与多功能干细胞都衰老都比较快,这使得它们的单位产能有限。正常细胞每一次分裂增值,DNF末梢都会变短一些,因此分裂到一定次数后就无法分裂了(自然条件下为20次左右),这个过程一般称之为细胞的衰老。
针对细胞易衰老这个问题,可以通过基因编辑来让细胞“长生不老”。美国著名细胞培养肉公司Memphis Meats采用的是诱导型多能干细胞(iPSCs),这种细胞经过了基因编辑,植入了KLF4与OLT4等基因片段,使得细胞增殖速度变快并且可以无限增殖。
美国的政府和消费者对基因编辑食品的接受度比较高,因此Memphis Meats可以采用基因编辑技术。但是由于欧洲的食品安全监管部门和消费者对基因编辑食品的接受程度比较低,因此总部位于欧洲的Mosa Meat没有选择通过基因编辑来提升产能,而是尝试控制培养容器内的环境(酸碱值、温度、浓度等因素)和培养液的成分来增加细胞的分裂次数(目前他们可以达到35次分裂)。
成纤维细胞增殖速度比较快,可以分化成肌肉细胞和脂肪细胞,相比起干细胞分化所需的引导物质比较少(成本优势),在通过一定的培育之后可以达到无限增殖的状态(不需要基因编辑)。以色列的细胞培养肉公司future Meat Technologies(FMT)采用的是这种技术,该技术的缺点是这种状态的细胞可能会被一些消费者与癌症细胞联系在一起。

不同细胞系的对比,图片来源:FMT首席科学家Yaakov Nahmias的一场分享会
培育各个可食用物种的细胞系是当前细胞培养肉领域的一个重要工作。新的细胞系的培育一般需要6-18个月,是一个费时又费资源的环节。在医疗研究和细胞工程研究领域,细胞库一般由政府赞助,但是这些细胞库里基本都是老鼠与人类的细胞,无法用于食用。出于研究目的的话,不同物种的细胞行为也不一样,研究成果无法共享。这样的背景下,专业的2B细胞系供应商会在产业价值链条上占有一定的地位。

细胞系的培养流程,图片来源:FMT首席科学家Yaakov Nahmias的一场分享会
2、培养液
培养液也是细胞在培养容器中生长的介质(Media),决定了产出的效率和质量,也是目前细胞培养肉生产流程中最主要的成本环节。一般来说,分化和增殖时需要用不同成分组成的培养液。
主流的细胞培养液最主要的成分是牛胎盘血清(fetal bovine serum ,FBS),FBS的价格非常昂贵,因此也造成了细胞培养液每升价格高达20美元。在大型培养容器中,生产1公斤的细胞需要使用10升的细胞培养液,也就是200美元,远高于饲养方法中每公斤肉2美元饲料的成本,因此如何降低培养液的成本成为了细胞培养肉降本中最有力的杠杆。
目前降低培养液的成本有两个方法,一个是使用植物成分来替代FBS,另一种是循环利用细胞培养液。
Mosa Meat和Eat Just都采用了植物成分的细胞培养液来降低成本。根据Just CEO的数据,植物基细胞培养液是Just的细胞培养肉产品的成本从2018到目前下降了40倍的主要因素。
目前市面上的FBS替代品都有一定的局限性,具体体现在无法达到FBS培养液一样高的细胞增殖生产效率。
植物基研发能力是Eat Just的一个强项,他们拥有in-house植物成分研发团队和植物基成分数据库,但他们目前也无法完全脱离FBS,去年2020年12月在新加坡通过细胞培养肉产品还是需要使用含有FBS培养液。
Mosa Meat的创始人Mark Post在去年年中时曾表示公司总共约70个员工中的20个在研究开发更具效率更便宜的细胞培养液,15个人在研究如何回收利用培养液。
细胞的排泄物(如氨)达到一定浓度后会杀死细胞,由于人体内有血管和肝脏所以可以“排毒”,培养的细胞组织由于没有血管和肝脏所以需要换培养液或通过一些手段来清楚细胞培养液内的排泄物。Future Meat Technologies就开发出了细胞培养液自循环清洁技术,把细胞培养液的成本下降了2-4倍。
细胞培养液供应商也是一个巨大的产业链机会,目前已有一些2B公司如Back of the Yards Algae Sciences、Multus Media、Future Fields、Luyef Biotechnologies与Agulos Biotech。此外一些专业的植物基成分研发公司也将具备很强的竞争力,目前已经出现了一些利用AI平台来发现植物中未知的营养素和风味的公司,如Brightseed与Climax Foods。
3、生物反应器

Future Meat Technologies的生物反应器,图片来源:食芯资本
细胞增殖分裂的过程叫生物过程(Bioprocess),生物过程决定了生产的效率。生物过程在生物反应器(Bioreactor,就是细胞培养的容器)中进行,与发酵蛋白发酵时用的生物反应器类似,它控制温度、氧气、培养液流动等要素,让细胞培养肉的规模化、过程可控化成为可能。
生物反应器的核心作用是让培养液转化成细胞的比例提高,这也叫“培养液转化率”,与传统畜牧业的“饲料转化率”相对。
比较常见的生物反应器有以下几种:
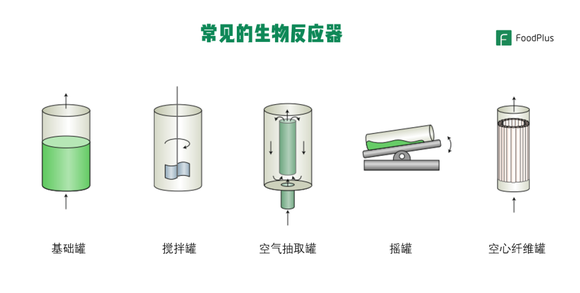
常见的生物反应器,图片来源:FoodPlus
这些生物反应器各有优缺点和不同的应用场景。搅拌罐一般用于哺乳动物的细胞培养并且对生产效率不错,但是容易撕裂细胞组织。空心纤维罐让细胞均匀生长在纤维的表面,平衡每一个区域的细胞浓度,但是这种设备比较贵,并且很难清理。这些生物反应器中最常见的是较为传统的搅拌罐与摇罐。
细胞培养肉开始大规模占领市场份额时会需要非常大量的生物反应器供给,这提供了一个产业链上的一个具有潜力的机会。目前已有一些2B的生物反应器供应商,如OSPIN、Celltainer Biotech、Cellular Revolution等。
未来生物反应器的研究开发与过程控制会需要多组学、生物工程学等多方面的研究作为理论基石,而通过电脑运算模拟的细胞行为将会扮演一个非常关键的角色。
4、支架
大多数动物细胞组织的生长聚合需要附着在一个“锚”上,支架(Scaffold)在细胞培养工程中就起到了这个锚的作用,给培养的细胞提供了生长所需的支撑网络。支架的材料需要能支持细胞摄取养分和营养物质、畅通排出细胞排泄物。早期细胞培养工程的目的多是生产医用的材料,因此使用的支架大多不可食用。目前业界正在研发新型的支架,这些新型支架可食用、具有特别的质地、味道、营养成分,可经受住烹饪。
常见的非动物来源支架材料如下:
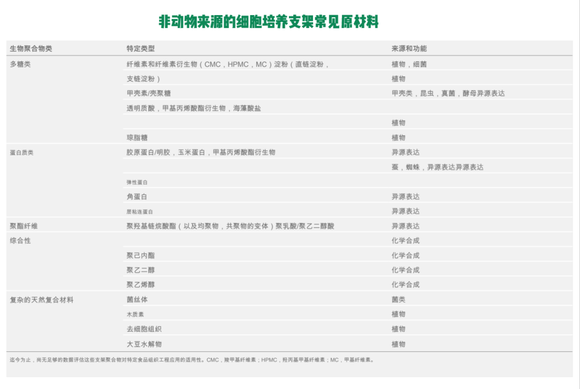
常见的非动物来源支架材料,图片来源:FoodPlus
支架无疑是产业链中的一个价值池。目前的支架解决方案在兼顾规模化生产、成本、产品最终形态上还有很大的优化空间,需要更多的研究与创新,未来的这些研究中用电脑运算模拟细胞行为会起到很关键的作用。目前已有一些2B的支架公司,如Atlast Food、Matrix Meats、Biomimetic等。
5、终端产品
由于生产技术与成本的限制,目前的离商业化比较接近的细胞培养肉产品多为“碎肉饼”形态。
在2013年Mosa Meat的产品的试吃会上,有试吃者这样评价道:“很干、味道有点淡,像是动物蛋白做的蛋糕”。试吃者这样评价的原因是当时Mosa Meat的产品只有肌肉细胞,没有脂肪细胞。
脂肪被认为是肉的味道的主要来源,也是人对肉上瘾的一个主要成分,脂肪在烹饪后会散发出非常独特的味道,这种味道实际上是一种结构非常复杂的碳氢化合物,这种化合物非常难通过化学方式来合成,因此细胞培养脂肪也被寄予了厚望。
Future Meat Technologies目前的人造肉产品是通过细胞培养脂肪与植物基肉混合得来,这种混合产品在兼顾了口味的同时能保持较低的成本,是目前一个从成本上比较接近商业化的细胞培养肉解决方案。
Mosa Meat目前宣称能生产100%成熟度的细胞培养脂肪,他们计划将这种脂肪与细胞培养肌肉混合得到目标产品。
此外目前也有一些2B的细胞培养脂肪公司,他们的潜在目标客户群体中很重要的一部分是植物肉公司。在知名的食品及原材料公司Kerry的一个调研中,超过2/3的植物肉公司表示愿意使用细胞培养脂肪来优化产品的口味、质地等属性。
3D打印是目前生产细胞培养全切肉(whole-cut)形态还原度最高的技术。以色列细胞培养肉公司目前已经可以通过3D打印技术生产带有筋脉和血管的全切产品,但是目前造价高昂,还无法商业化运用。目前已有许多人造肉公司重点关注3D打印技术,如SavorEat与Redefine Meat。倘若3D打印在细胞培养肉领域中大规模运用,3D打印机供应商也会在该产业链中占有一亩三分地。

Aleph Farm的全切肉产品,图片来源:WSJ
6、产能和成本
细胞培养肉技术目前已呈现出不错的产能效率,对比传统畜牧养殖方法极大的生产灵活性,成本在近年来已可观地降低。
以Mosa Meat为例,目前他们利用0.5g的活体组织就可以生产出2000kg的肉,利用一个一立方米容积的生物反应器,一年可以生产出10-20吨的细胞培养肉。这种产能对应的细胞的分裂次数为30次左右,根据海佛里克极限(Hayflick Limit),正常体细胞的分裂次数极限应为50次左右,目前的情况距离理论极限还有一段距离,而细胞分裂每提升一次都会带来指数级的产量增加。
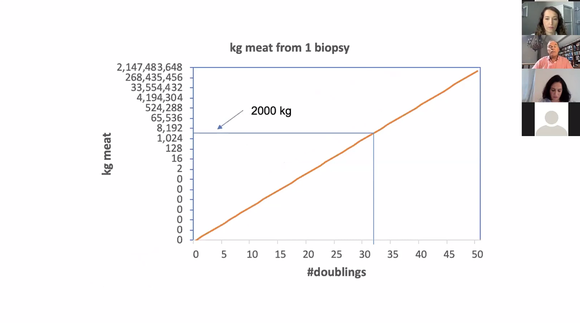
细胞分裂次数与产量的坐标系,来源:New Food Conference webinar 2020
传统畜牧方法养一头牛到成熟需要46个月,鸡需要30-60天,而细胞培养肉技术的生产周期则是2周左右(10-12天培养成熟,2天左右清洗生物反应器)。生产的灵活性使生产者可以灵活安排需要生产的肉类类型,牛肉、猪肉或禽类,并且可以在当地生产节省运费,面对需求的不确定性的风险也更低,这些便利性实际上一定程度降低了生产者的风险和成本,这种降本也可以进一步传导到产品价格上。
价格方面,尽管目前细胞培养肉成本还比较高,但是我们已经看到了非常大幅度的减少,未来预期还能进一步下降。在使用“细胞培养脂肪-植物基”的人造肉解决方案后,目前Future Meat Technologies每份鸡肉产品的价格为7.5美金(约113克),这个价格是2019年的/15,7年前的1/28000。2013年Mosa Meat的第一块细胞培养肉饼造价32.5万美元,他们预期短期内可以把这个成本降到11美元。

细胞培养肉消费者接受度调研,整理:FoodPlus
在翻阅了十数个关于细胞人造肉接受度的消费者调研后,我们得出了以下几点消费者市场观察:
1、提供的关于细胞培养肉的信息越丰富,受访者的接受度就越高;
2、在沟通中突出细胞培养肉的环境意义与真肉还原度等积极信息能提高受访者的接受度;
3、在沟通中强调细胞培养肉的科技感不能有效提高受访者的接受度,使用“实验室肉”这样的名称甚至会降低受访者的接受度;
4、使用“净肉(clean meat)”这样的名称能提高受访者对细胞培养肉的接受度;
5、接受度上,整体来看,中国>印度>美国,男性>女性,年轻群体>年长群体,杂食者>素食者;
6、目前整体消费者接受度不算高;
7、植物肉的接受度目前略好于细胞培养肉。
业内人士普遍认为:细胞培养肉目前的监管阻力大于技术阻力。许多几年前进入这个领域的创业公司目前的产品已经可以到商用的产能和价格了,目前他们面前最大的阻碍是各国的监管政策都还没有落地。
这个章节我们梳理了目前一些主要市场政府对细胞培养肉的态度以及相关政策动向。
1、国外
新加坡、美国、欧洲、以色列是在细胞培养肉监管政策的推动上比较积极的国家。
新加坡政府最快通过世界上第一个细胞培养肉食品安全审核是意料之中的事情。城邦之国新加坡94%的食品供给来源于进口,食品供应的稳定与安全问题一直是新加坡迫切需要解决的难题。因此,新加坡政府组建了一个120人的食品供给创新机构,以推动新加坡的食品供给系统升级。新加坡计划到2030年,全国30%的食品供给将来自于国内。目前多家细胞培养肉公司都在与新加坡相关监管部门接洽并合作推动产品审核,预计很快还会有其他的细胞培养肉产品在新加坡通过审核。
美国的细胞培养肉监管推进步伐已经远超其以往对新食品的监管推动速度。在2019年3月,美国的两大食品安全监管部门FDA(美国食品药品监督管理局)与USDA(美国农业部)宣布了双方会共同监管美国的细胞培养肉行业。那之后,FDA已经推出了细胞培养海鲜申请需要的材料的清单(海鲜不归USDA管,所以推动进度会比细胞培养肉更快)并为申请者进行辅导,USDA相关发言人表示他们也非常接近推出类似的清单。
BlueNalu发言人在2021年1月时曾表示他们在一年半前就开始与FDA合作推动监管审核,目前很有希望会在今年获得审核并推出商业化产品。另外,民主派领袖拜登上台后,市场也普遍认为这会利好美国替代蛋白的监管推动。

2019年3月,FDA与USDA宣布双方共同监管美国的细胞培养肉行业,来源:USFD
值得注意的是,2020年7月,肯德基在俄罗斯与当地的一家食品科技企业3D Bioprinting Solutions宣布正在合作研发细胞培养肉,将于2020年秋天提交审核申请。许多业内人士认为,如果俄罗斯通过了细胞人造肉的安全审核,这将会极大的推动中美相关政策的制订进度。
在美国,传统肉产业方已经发起了自卫行动,在监管层面他们做出的努力是游说各州政府禁止细胞培养肉被标签为“肉”。2018年8月,美国密苏里州率先通过了相关法案,随后,美国十数个州跟进了类似的法案。
美国和新加坡之外,欧洲的许多国家、加拿大、以色列、韩国、日本在细胞培养肉行业的推动上也比较积极,除了在积极准备相关监管政策外,一些政府组织还为相关企业和机构提供了资金帮助,这里不一一展开。
2、中国
目前中国在细胞培养蛋白领域还没有相关的政策和条例动向,但我们有理由相信中国有对替代蛋白施行鼓励政策的潜在可能性,并且这种可能性不低。
由于是全球最大的石油进口国,出于国家能源安全、能源结构、政治、军事等方面的考量,中国在新能源领域给予了非常强的战略引导指示,如“预计到2020年,中国在新能源领域的总投资将超过3万亿元”、“到2025年,新能源汽车新车销售量达到汽车新车销售总量的20%左右”等等,这期间给予B端和C端的政策补贴都极大的推动了新能源相关领域的大跨步。以新能源汽车为例,制造商有生产补贴和税收优惠,消费者有新能源车牌、免购置税、不限行等优惠。
而中国同样也是全球最大的肉类产品消费国、最大的肉类产品进口国,进口量年增长率维持在两位数,这种情况给国家鼓励替代蛋白提供了土壤。
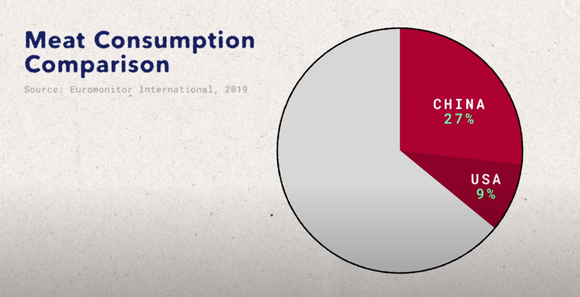
各国肉类消耗占全球肉类消耗的比例,来源:Euromonitor
我们捕捉到了一些事件,把它们串起来或许我们能得到一些具有风向标意义的信息。
2016年中国卫生部起草的新居民膳食指南中特别强调建议了中国13亿人口应该每人每天食用40克到75克的肉(目前的基础上减半),该指南每十年发布一次,这次指南强调减少肉摄入除了改善公众的健康状况,也意图配合国家环保战略,为温室气体排放量的大幅减少提供了机会。畜牧业占了地球年总温室气体排放量的50%左右,如果能减少一半的畜牧业牲口存栏量,将对中国的碳排放量缩减做出极大贡献。
2017年中国政府与以色列政府达成了一个3亿美元的交易协议,意在促进以色列环境友好的能源与农业食品科技出口到中国。
2020年,全国政协委员孙宝国带着“关于加快细胞培养肉发展战略部署”的提案上了全国两会,建议加快建立和完善细胞培养肉产业监管体系和法律法规。

细胞培养肉技术与传统养殖生产肉类方法资源使用的对比,来源:Environmental Impacts of Cultured Meat Production
细胞培养肉技术生产单位重量肉类的温室气体排放量是传统畜牧业4%、占地面积是传统畜牧业的1%、水使用量是传统畜牧业的4%-18%,生产效率方面则远远领先于传统畜牧业,完全没有可比性。
作为一个能解决多方面资源问题又能契合国家环保大战略的农业食品技术,我们完全有理由相信国家会把对新能源发展战略的重视程度复制到替代蛋白发展战略上来。可以想象一下某个红头文件中出现“到2030年,新型肉类占总肉类消费量的20%左右”这句话时会给供给端带来怎么样的冲击波。