尽管顺势疗法的原理缺乏科学依据,但是这并不妨碍它大行其道。

编者按:FDA名词解释,FDA是食品药品监督管理局(Food and Drug Administration)的简称。FDA是国际医疗审核权威机构,由美国国会即联邦政府授权,专门从事食品与药品管理的最高执法机关;是一个由医生、律师、微生物学家、药理学家、化学家和统计学家等专业人士组成的致力于保护、促进和提高国民健康的政府卫生管制的监控机构。其它许多国家都通过寻求和接收 FDA 的帮助来促进并监控其本国产品的安全。

顺势疗法(Homeopathic)是一种替代疗法,风靡美国。1796年,由山姆·赫尼曼按其以同治同理论所创。此理论指,如果某个物质能在健康的人身上引起病人患某病时的病症,将此物质稀释震荡处理后就能治疗该病症。例如洋葱会引起打喷嚏,多次稀释震荡后的极微小洋葱,就能治疗打喷地症状为主的鼻炎。
很显然,此疗法为伪科学,是错误认为是科学的一个信仰系统。顺势疗法对任何病症均无作用,大型研究均发现顺势疗法不比安慰剂有效,指出该疗程带来的任何正面感觉,都只不过是安慰剂效应及人体的自然康复。
在编号7682299的案例中,2010年8月1日,一位母亲为了缓解女儿的出牙疼痛,给她喂服了3片顺势疗法的出牙药片。然而几分钟之内,这个可怜的小宝宝停止了呼吸。
“在我给我女儿喂了3片Hyland’s公司的出牙止痛药后,她癫痫发作并且失去意识,然后在大约30分钟内停止呼吸,”这位母亲事后向美国食品药品监督管理局(下称FDA)陈述当时的情况,“我只能给她做口对口心肺复苏来恢复宝宝的呼吸,然后立即将她送到医院。”
这位母亲所使用的药品来自Hyland’s公司,该公司鼓吹自己“致力于安全、有效和自然的治疗手段”以吸引为人父母的消费者尝试这种替代疗法。FDA在此事件以后也很快获悉了更多关于该公司的儿童出牙产品的信息。FDA的工作人员也将编号7682299视作一个结果比较幸运的案例。

Hyland顺势疗法出牙药片外包装,注明缓解儿童出牙疼痛症状、无副作用、100%纯天然、药片可速溶服用信息
STAT网根据“信息自由法案”规定,从FDA处得到了对该公司调查的记录报告,得知了事态的严峻程度更甚上面的案例。那些服用了Hyland’s公司出牙产品的孩子们会有抑郁的倾向甚至有死亡案例,他们还可能出现反复的癫痫以及精神狂躁症状。很多孩子因此被送往医院,医护人员着手调查,试图找到他们四肢抽搐的原因。
在2006年至2016年这10年期间,FDA已经收集了超过370名因使用Hyland’s公司生产的顺势疗法出牙药片或出牙凝胶而导致“不良反应事件”的儿童案例报告,其中的出牙凝胶是直接在孩子的牙龈上使用的,其作用类似于出牙药片。据FDA的记录显示,目前已有8名儿童在服用Hyland’s公司的产品后死亡,但是FDA仍旧还在调查是否是这些产品直接导致了孩子的死亡。
此外FDA还在调查另外两起与出牙药物相关的死亡案例,但是没有透露产品生产商或者提供案例报告。
2016年9月FDA发出警告称顺势疗法出牙药片和出牙凝胶可能对儿童存在安全隐患,建议消费者停止购买和使用 。随后Hyland’s公司表示他们将停产儿童出牙产品。但是这些产品在之后数月仍然在一些商店的货架上售卖,另外网上也依旧可以买到。这意味着,全美范围内仍然有很多家庭会使用到该产品。
Hyland’s公司位于洛杉矶,是一家已有114年历史的私人公司,也是美国顺势疗法市场的龙头企业。该公司坚称自己的产品是十分安全的,并表示FDA并没有确凿的科学证据证明那些儿童的癫痫症状及其他并发症与他们的产品有直接关系。
FDA发言人Mary Borneman表示:“尽管没有直接证据,但是不意味着孩子对这些产品没有敏感性,孩子们有很多身体部位是十分敏感的,我们还需要进一步仔细观察。当然,这也并不是在谴责这家公司的所有生产线。”
每一个FDA案例编号的背后都有着愤怒和心碎的父母们。但是在STAT网的这次调查当中人们才得以第一次看清这些案例报告,这也让人们对相关监管机构在这些事件的反应速度上提出了质疑。
足足等了四年时间,2010年FDA才发出有关出牙药片的警告,责令Hyland’s公司对他们的药物进行整改。从那以后至今的7年当中,仍然有层出不穷的不良反应报告指向Hyland’s的儿童出牙产品。
“FDA完全可以将监管重锤一直放在这公司身上,”来自一个公益性的公众健康研究团体的律师Sarah Sorscher无不责备地说到,“但是它并没有这么做,在出现了婴儿的死亡和住院报告时他们才有所行动,这样的拖延和不作为真的难以让人接受。”
FDA的一位发言人对他们机构就此事的处理方式进行辩解。
“尽管这些产品的不良反应报告为我们提供了一些产品信息,及特定产品使用者因之被造成的严重伤害和死亡案例,但我们仍要指出的是,这些信息仅意味着我们还需要做进一步的分析检测,它们无法构成证明该产品存在问题的确凿证据。”FDA发言人Lyndsay Meyer女士在一次声明中表示。
虽然FDA很难证明Hyland’s的产品伤害了儿童,但一些医生毫不质疑这些产品所具有的危险性。
在2011年9月15日的编号462749案例中,一位医生递交了自己关于Hyland’s药品的手书笔记,表明他的一个5个月大的女婴患儿在服用Hyland’s的出牙药片后陷入了长达45分钟的昏迷。
“我确定这并非过敏反应,”该医生在笔记中写到,“我希望你们报道这件事,并与FDA取得联系,这样我们才可以着手调查,让这个危险又不受管制的产品不再上架销售。”
一位母亲在对Hyland’s公司的控诉中写到,她的儿子在服用他们的产品后瞳孔扩大得就像“长着大黑眼的大理石 ”。另一位母亲则描述自己的女儿在服用出牙药片后出现了持续的癫痫症状,她愤恨地向Hyland’s公司表示:“我真是打心底地痛恨你们!”
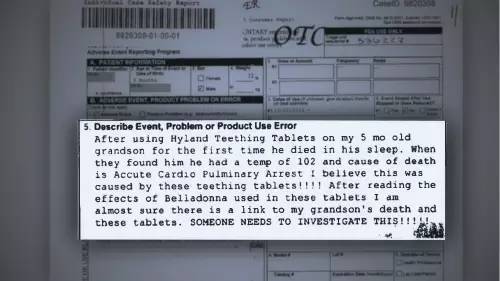
药品不良反应、问题及使用错误叙述
我5个月大的孙子在第一次服用Hyland’s公司的出牙药片后,就在睡梦中死去了。当我们在注意到的时候,他的体温已经102华氏度(38.9℃)了,致死原因是急性心肺阻塞。我相信这一定是那些出牙药片导致的。我在看了颠茄在这些药片中起到的作用后,我几乎可以肯定我孙子的死和这些药片有关联。请一定要有人来调查这些药!
Hyland’s公司及其母公司都是标准的顺势疗法公司,他们被认为在顺势疗法市场中占有主要份额。其CEO John P. Borneman的家族已经在这个行业打拼数代,同时他还任职行业协会的主席,该协会曾颁布了顺势疗法药典,这在顺势疗法业内中被视作有如圣经一般的纲领。
Hyland’s公司生产和销售着数十种顺势疗法产品,用于治疗缓解头痛、压力过大、睡眠障碍、过敏、流感及其他健康问题。
正如其他顺势疗法所采用的原理一样,Hyland’s公司的产品也遵循着“如果某天然物质的原始形态能使健康人患病,那么将此物质高度稀释处理后就能治疗该病症”的理论。
尽管顺势疗法的原理缺乏科学依据,但是这并不妨碍它大行其道。
顺势疗法现如今已发展壮大成为年产值高达数十亿美元的产业。它的产品在世界范围内都有着可观的销量,从好莱坞老牌巨星雪儿到查尔斯王子都是顺势疗法的忠实拥趸。这个行业同时还有着巨大的政治影响力:它在美国国会及FDA这些年颁布的诸多法规中都能得以法外豁免。
与制药公司的产品不同的是,顺势疗法产品无需证明它们在治疗某病症上的有效性,这个差异在产品上市前的阶段尤为明显。由于不良反应报告通常被看做是只反映了实际情况的冰山一角,它们提供的信息可能远不够充分来进行彻底调查,所以这给FDA的药监部门出了个大难题,究竟如何判断这些产品在上市后存在着安全隐患呢?
“如果我是一名急诊室的医生,有一家人带着有癫痫症状的患儿来求诊,我可能真的难以得知其顺势疗法产品使用史。”哈佛大学的毒理学家Edward W. Boyer博士无奈地说。
因为在有些情况下,有的父母认为类似Hyland’s出牙片和出牙凝胶等顺势疗法产品基本没有可能引起并发症,所以他们在带孩子就诊时不会提及曾使用过这些产品。由于没有充分的证据表明产品确实存在问题,故FDA缺少它所必须的执法手段。
Karinna Talbott是一位家住科罗拉多斯普林斯的26岁年轻妈妈,据她表示,Hyland’s的出牙产品光明正大地标榜自己是“纯天然的”,这在很大程度上打消了她的顾虑。
“当我们第四个孩子出生后,大概在他三个月大的时候开始长牙,那时我们就在考虑能为孩子做点什么减轻他出牙的痛苦呢。” Talbott女士回忆到,“后来有人给我们推荐这个出牙药片,我们就想着,要不就试试看吧。”
然而不幸的是,她的儿子在服用该出牙药片后不久手部就出现了抽搐症状。
“起初我们并没有把宝宝的抽搐和出牙药片联系在一起,” Talbott女士坦言,“但是他的症状越来越严重,胳膊和脚也都会抽搐,甚至有时候四肢同时抽搐。”
Talbott说医生一开始也并不明确是什么原因导致了这个症状。但是当他们不再给孩子喂服出牙药片后,这个癫痫症状也随之消失了。
“一位神经科医生告诉我们,可能是我宝宝对这个产品有些敏感。”

和他的爸爸在科罗拉多斯普林斯的家中
“致命茄科”
在对Hyland’s的出牙产品进行调查的过程当中,FDA着重调查的是该产品中的一种阿托拉颠茄成分,这是一种被俗称为“致命茄科”的草药。
产品中的该成分是被稀释过的,理应不该有任何毒副风险。但是在2010年的调查中,FDA的设备检查人员指出Hyland’s的生产过程不符合相关标准,并且还发现他们的产品中颠茄含量并不均等。
于是FDA发布了一则公共警告,披露出“关于儿童所服用的该出牙产品与其中所含的颠茄成分导致不良反应的一致性报告”。
该警告还指出,由于婴儿身体对毒素的扩散和响应速度与成人不同,所以他们“对药物中含有的神经毒素十分敏感”,而且“他们的皮肤和口腔黏膜吸收颠茄成分的速度尤其快。”
尽管Hyland’s公司依旧坚称他们的产品是十分安全的,但他们还是自愿将该产品下架并进行生产整改。
FDA发言人Borneman女士表示:“这样的处理方式是很正确的,父母们再也不必为这个产品是否安全感到忧虑了。”
这几年FDA记录在案的该产品严重不良反应报告数量在持续攀升着。已有一些儿科和神经科医生开始认为成因正是这些出牙药片和凝胶。许多家长向FDA写信投诉,质问为何这些问题产品还依旧没有下市。
2012年2月13日,一位母亲发现该产品疑似导致自己的儿子发作了好几次癫痫,她向FDA控诉道:“我的儿子也曾服用过3片那个出牙药片。这个产品有增无减的流行程度真的令我咋舌,我们很多父母其实很缺乏相关的知识,同时这些商品上也没有任何警示标签。如果非得允许其继续销售,那么你们有关部门请采取一些必要的措施,比如给它们贴上警示标志,很多父母都需要这样的提醒。”
2016年9月30日,FDA在发出对Hyland’s公司的警告的同时,也宣布他们正在进一步调查更多的不良反应事件,并建议消费者停止使用Hyland’s公司及其他顺势疗法出牙产品,处理已经购入的相关产品。包括Target和CVS在内的一些曾售卖Hyland和其他顺势疗法出牙产品的商家也都响应该警示,将这些产品下架。
FDA还再次要求Hyland’s公司召回相关产品,但是这一次该公司却坚定自己的立场不予采取行动,而FDA是没有权限强制他们召回顺势疗法产品的。
FDA发言人Borneman女士表示该公司在2010年后推出了一套名为“药物警戒计划”的产品安全审查系统,来证明他们的产品是安全的。
“顺势疗法的安全边界是很模糊的,”她说,“我们的检测旨在确保每一瓶药片中都没有含有过多的颠茄成分。”
与此同时,Hyland’s公司决定停止生产该出牙药片。在给消费者的公开信中,他们表示FDA的安全警示反而“造成了父母们的迷惑”。
该公司对此作出回应:“FDA让消费者不得不面对这样相互矛盾的信息,你们只得决定究竟应该信任哪边,这对你们而言只是沉重的负担,并且也破坏了FDA自己的威信。请大家继续相信Hyland’s公司,继续使用我们的产品,包括现在你已经买到的产品,它们都是绝对安全的。”
几周前的1月27日,FDA再次发出警告,他们在实验室分析发现Hyland的顺势疗法出牙药片的颠茄成分不均 ,有时甚至远超过他们标签上标注的含量,这可能对儿童造成不必要的风险 。他们敦促消费者不要使用该产品,如果发现孩子在服用该药后出现癫痫、呼吸困难、嗜睡、肌肉无力、皮肤潮红、排尿困难或其他不良反应,请立即上医院就诊。
FDA同时还表示根本也没有确切证据能表明这个产品是确实有效的。

有孩子在服用该出牙片两周后死亡,尽管这个商品早已被召回,但是市面上还仍有售卖
出于对颠茄毒性和层出不穷的不良反应事件的担忧,一些批评人士和父母对FDA颇有微词,他们认为FDA应该在Hyland’s公司这些事件上采取更为迅速的行动。
同时他们也承认,这些事凸显出了当面对顺势疗法产品时,监管部门的权限就存在着盲区。在FDA可以对该公司的库存进行调查、征收罚款或勒令停产之前究竟需要有多少患儿的案例报告,这并没有公式或者官方标准可遵循。
批评人士指出,由于顺势疗法产品通常采用高度稀释的物质,这让他们总被FDA搁置一旁。
Aaron S. Kesselheim博士去年在新英格兰医学杂志上发表了一篇关于顺势疗法的论文,他指出:“顺势疗法在相关部门中的监管优先度很低。因为这些产品常采用惰性或高度稀释的物质,长期以来FDA总是在监管它们时表现得不那么积极。它们对消费者造成的损失主要是浪费金钱或者让人们没有用上真正有效的产品。”然而在Hyland的产品问题上,Kesselheim博士认为正是颠茄成分的毒性所造成的相当大的安全隐患推动了FDA的监管举措。
FDA之所以对这些事件反应缓慢是事出有因的,他们在人员配置上存在一个问题:他们会安排卫生干事对每一份生产企业的报告进行审查,但却没有安排人员去定期跟踪患者、患者家属和医生,以获取采取强制执法手段时所需但现在又缺少的报告。
“过分去苛责FDA从2010至今行动缓慢真的不有失公允吗?”佐治亚州立大学助理法学教授Patricia Zettler质问道,他曾任FDA的法律顾问。“我认为在面对这些顺势疗法产品和其不良反应报告时,FDA自身也处在一个很艰难的处境。因为这些都不能成为不良反应直接与产品相关的充分证据。”
Zettler教授补充说明:“我的意思是,对,这些产品看起来的确应该得到FDA的有效监管。但是到底在收到几份癫痫病例报告后就足够他们采取行动呢,两份三份还是十份?这真的很难决断。在有足够明朗的信息时迅速行动,和防止在并非由该产品引起问题时反应过度,FDA需要在这两者之间保持好微妙的平衡。”公众健康研究团体的Sorscher律师坦言,当事件上升到刑事案件时追究起来费时费力,所以FDA更倾向于相关企业能自觉遵守规定。
她指出:“他们并没有相关的法规来明确表明这种成分是不安全的,禁止所有人售卖。或许现在就是国会要求FDA建立相关规定的好时机,来彻底禁止这种产品的生产销售。”
FDA和Hyland’s公司之间的僵持局面让康涅狄格州民主党议员Rosa DeLauro大为光火,她于上周(2月16日)提交了一份名为“不安全药品召回法案”的议案,该议案将重塑FDA在面对顺势疗法产品时的权威地位。当前FDA仅在对医疗器械、食品和生物制品等产品上有强制召回权。
所以,当药品出现问题时,FDA只能发出警告,依靠企业的自觉性来召回药物。当然很多企业会在自己的药品存在安全隐患时重视FDA的警告。然而有些企业即便在面对确切无疑的证据表明他们的产品可能造成使用者生病或死亡时,也依旧拒绝召回他们的产品。
DeLauro议员愤怒地表示:“Hyland’s公司对FDA诸多安全健康警告熟视无睹,并拒绝召回他们的问题产品,这是非常无耻的行径!”她 随后补充道:“这家公司选择了优先考虑自己的利益和名声,而不是我们孩子的安全健康。”
“而现今的情形是,FDA为了对诸如Hyland’s公司的企业采取措施,还不得不诉诸艰巨繁琐的法律程序。我们难以接受这种费时费力的过程,这分明是在为美国民众的健康安全埋下隐患。我认为填补监管部门强制召回权的漏洞是势在必行的,国会应当采纳我的提案,建立法规让这些威胁消费者健康安全的产品彻底从市场上消失。我们美国公民有权利知道他们正使用的产品是安全的。”
对于编号10723317案例中的父母而言,任何措施都已于事无补了。这位母亲报告说,2014年7月9日,她仅9个月大的女儿在第一次服用两片被碾成粉末的出牙片后死亡。她当时给女儿喂了药片和一杯水,然后哄她睡觉。45分钟后这位母亲来检查她女儿,等待她的却是婴儿床里女儿冰冷的尸体和身旁的一滩呕吐物。事后五个月,她在网上阅读到关于婴儿服用颠茄可能引发癫痫的报告后,她联系了Hyland’s公司。
一位Hyland’s公司的员工在提交给FDA的报告中说明:“该客户并没有提出退款或者换货要求。”同时Hyland’s公司方面还指出,由于该客户已经丢掉了那瓶药,所以已经无法对其做分析检测了。
最后Hyland’s公司的结论是:“由于该报告人能提供的信息实在有限,已经无法再针对此事件做进一步调查。”

文章来自于STAT,动脉网记者唐大彪进行了编译,不代表动脉网观点。
动脉网所刊载内容之知识产权为动脉网及/或相关权利人专属所有或持有。未经许可,禁止进行转载、摘编、复制及建立镜像等任何使用。